-Prefazione – Mario Mandici ci accompagna nel viaggio attraverso la chimica dell’acqua in acquario: pH, KH e GH.
Un viaggio in cui cercherà di rendere più facile per quanto possibile la comprensione di concetti indubbiamente di non facile comprensione per i non addetti ai lavori, come il sottoscritto, ma che sono di aiuto per capire molte dinamiche che regolano la biologia degli ecosistemi acquatici.
Il pH
Prima di entrare nel vivo di questo importante parametro vorrei fare una premessa. Uno degli argomenti più dibattuti nei social dell’acquariofilia è il valore del pH dell’acqua in cui tenere i nostri pesci. Spesso di scatenano acerrime discussioni al pari di quelle calcistiche e politiche. È vero che ormai molte specie provengono da allevamenti che poco tengono a rispettare questo parametro ma è anche vero che restituire a loro ciò che gli appartiene non è errato … anzi sarebbe preferibile. Non confondiamo la mutazione genetica, processo che richiede lunghissimi periodi di tempo, con la capacità di un essere vivente di adattarsi ad un determinato ambiente. È anche vero che ci sono specie di pesci che si trovano in natura in diverse zone geografiche dove il pH può essere molto diverso da una zona all’ altra. Un esempio lampante sono i Guppy. Il discorso cambia totalmente quando abbiamo a che fare con specie d’ importazione diretta, per queste rispettare il pH è un obbligo! Personalmente preferisco sempre rispettare i valori chimici delle acque di origine come pure preferisco rispettare i biotopi.
Ma cosa si nasconde dietro questo simbolo?
Esso, senza entrare nei tecnicismi di formule matematiche, rappresenta la concentrazione di ioni idrogeno H+ o se preferite dello ione idrossonio H3O+ presente in acqua.
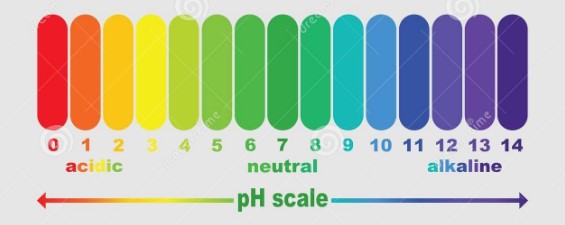
Il Ph si esprime attraverso una scala convenzionale detta scala del pH cha va da 0 a 14. Il valore 7 rappresenta un’acqua neutra. Valori inferiori esprimono l’acidità e valori superiori l’alcalinità.
Metodi di misurazione
Phmetro digitale. Si va da quelli più sofisticati ma dai costi elevati a quelli più a portata di portafoglio. Tutti comunque vanno calibrati con una certa frequenza (dipende dall’ uso ma direi che ogni 15/30 giorni è un tempo ragionevole) usando soluzioni tampone a pH 4.0 e pH 6.86 oppure pH 6.86 e pH 9.0 nel caso di acquari dove necessita avere un pH superiore a 7.0. Non entro nel merito di come funziona un pHmetro per complessità della materia. Il bulbo non deve mai seccare e mai essere conservato in acqua distillata. Quando fate la prima taratura prendete la soluzione a pH 4.00 e imbibite del cotone idrofilo che avrete messo nel cappuccio di chiusura del pHmetro in modo da mantenere il bulbo umido. Diversamente l’elettrodo a membrana (bulbo) tenderebbe a perdere la sua velocità nella risposta ma anche la precisione. Quando effettuate la misurazione del pH prelevate il campione di acqua in un bicchierino ed immergetevi il pHmetro. Il valore di lettura sarà più stabile nel breve tempo.
- Test a reagente liquido. Questi test usano degli acidi o delle basi di natura organica sciolti principalmente in un veicolo idro alcoolico capaci di virare il loro colore in funzione del valore del pH. Fra i vari coloranti impiegati in acquariologia quello più interessante è il blu di bromotimolo perché varia la sua colorazione in un range di valori ristretto con variazioni cromatiche di 0,2 unità di pH.

- Test a striscette. Sono da scartare perché spesso imprecisi e soprattutto perché presentano un range di valori troppo ampio non solo per il Ph ma anche per altre misurazioni.
Come modificare il pH
Abbassare il pH
- Soluzioni di HCl o acido citrico, rappresentano un metodo efficace e pratico che sconsiglio perché si rischia di fare danni per una brusca variazione del pH, meglio preferire metodiche più naturali e soft.
- Filtraggio attraverso la torba sfruttando la sua capacità di rilasciare acidi organici diprotici (sono quelli che rilasciano 2 ioni idrogeno abbassando nel contempo anche il KH (ricordate la sua azione tampone?). Attenzione che se il KH è già basso di suo si rischia di acidificare troppo. Inoltre la torba rilascia preziosi acidi umici e fulvici utili alla salute dei pesci ma che conferiscono all’ acqua quel colore ambrato non da tutti apprezzato.
- Decotti di foglie di catappa o di pignette di ontano molto lenti nell’abbassare il pH, poco durevoli e poco controllabili.
- Uso della CO2. È il sistema più efficiente e controllabile con minime fluttuazioni tra il giorno e la notte se lasciato funzionare 24H/24. Inoltre non dimentichiamo che la CO2 rappresenta la fonte di carbonio inorganico utilizzato dalle piante per la produzione di quelle sostanze plastiche come la cellulosa durante la fotosintesi clorofilliana.
Alzare il pH
- Anche in questo caso è possibile fare ricorso a prodotti specifici ma preferiamo una chimica diversa per approcciare a questa esigenza.
- Usare prodotti che intervengono sull’ innalzamento del KH vista la stretta relazione che c’è tra l’azione tampone degli idogeno carbonati/carbonati ed il Ph.
- DIY (fai da te), mai usare sali contenenti sodio come il bicarbonato vista la tossicità del Na verso le piante che tollerano male concentrazioni superiori ai 40 ppm. Usiamo il corrispettivo sale di potassio (KHCO3).
- È sufficiente ridurre la micronizzazione della CO2 per vedere un innalzamento del pH mantenendo il KH a valore costante.
Ma cosa succede quando micronizziamo CO2 in acqua?
H2O + CO2gas <-> H2CO3 <-> H+ + HCO3
ma possiamo anche scrivere
H2O + CO2gas <-> H+ + HCO3
L’ acido carbonico in soluzione si dissocia quasi completamente in ioni idrogeno e idrogenocarbonato che rappresentano i prodotti della reazione della CO2 micronizzata in acqua.
Lo ione idrogeno H+ prodotto nella reazione è responsabile dell’abbassamento del pH
C’è una stretta relazione tra pH e KH.
Il KH per la sua attività tampone tende a contrastare variazioni di pH per aggiunta di piccole quantità di sostanze acide per cui se volete ridurre il pH qualunque sia il metodo usato è sempre preferibile abbassare prima il KH evitando di andare sotto i 3 dKH. Per valori di KH inferiori a 3 occorre porre maggiore attenzione. Per chi usa la CO2 per abbassare il pH significa risparmiare sull’ erogazione del gas. Alzare il KH significa aumentare l’azione del tampone del KH per cui seguirà un aumento del pH.
La durezza KH
L’ altra misura che andiamo a determinare spesso è il KH ovvero la durezza carbonatica di un’acqua che è condizionata dalla presenza di idrogenocarbonati (HCO3–) e carbonati (CO3-). Il test del KH in realtà non misura la concentrazione di tutti gli idrogenocarbonati (quindi non solo quelli di Ca e Mg) ma bensi l’alcalinità ovvero la capacità dell’effetto tampone che si ha sul pH da parte di questi. L’ effetto tampone del HCO3– tende ad impedire variazioni brusche del pH per aggiunta di ioni idrogeno. Questo ci fa capire che se il KH è molto basso (< o = 2) basta una piccola aggiunta di una sostanza acida per abbassare anche bruscamente il valore del pH. Invece valori alti di KH si opporranno agli abbassamenti del pH per aggiunta di piccole quantità di acido. Quindi il KH è un parametro importante per decidere come stabilizzare il pH e/o modificarlo più facilmente sfruttando la CO2 micronizzata o l’effetto acidificante delle foglie in particolar modo quelle di catappa o le pignette di ontano. In base al tipo di acquario che andremo ad allestire sarà importante operare anche con il giusto valore del KH. Immaginate una vasca black water o comunque un acquario dedicato ai caracidi o ai ciclidi sud americani come a tante specie del sud est asiatico. Un KH basso intorno a 3 max 4 dKH ma anche intorno a 2 dKH per chi è bravo a gestire la micronizzazione con CO2 renderà semplice ottenere un acquario con pH intorno al 6.0 – 6.5. Chi alleva caridine cantonensis sa che il KH non dovrebbe superare 1 dKH, viceversa un acquario per ciclidi africani (Malawi piuttosto che Tanganica) richiederà un KH alto (intorno a 10 dKH) per assicurare che il pH non scenda mai sotto il 7,8. Ricordatevi che c’è un stretto legame che lega il KH al pH.
In un acquario mediamente il rapporto KH:GH deve essere di circa 1:2 ma anche questo dato è relativo perché molto dipende dalle specie di pesci che abbiano. Come già detto, coloro che utilizzano acqua di rete devono fare molta attenzione quando trovano un valore di KH>GH. Questo significa che l’acqua è ricca di carbonati di sodio (Na2CO3) in quanto il magnesio (Mg) è legato essenzialmente ai solfati che non incidono sul KH mentre il potassio (K) è quasi sempre irrilevante come contenuto nelle nostre acque. Il sodio quando supera la concentrazione di 40 mg/lt incomincia ad avere un effetto negativo sulle piante. Viceversa quando un’acqua di rete ha un GH>>KH questo indica una buona presenza di magnesio (Mg) presente sotto forma di MgSO4. La grande differenza tra GH e KH non è dovuta a CaSO4 perché scarsamente solubile in acqua né a Ca (HCO3)2 perché i bicarbonati avrebbero dato un KH alto.
Abbassare il KH: Per questa operazione dobbiamo intervenire con i cambi parziali fatti esclusivamente con la RO (RO = reverse osmosis) ponendo attenzione a non abbassare il KH di oltre 2 gradi giornalieri in quanto si potrebbe avere una modifica repentina del pH.
Come faccio a calcolare la quantità di RO ? Niente di più semplice.
- C1xV1=C2xV2
- V1-V2= volume acqua acquario da sostituire con RO
dove C1=dKH acquario, V1=volume netto acquario, C2=dKH desiderato, V2= volume acquario da mantenere.
Facciamo un esempio: supponiamo che il nostro acquario ha un volume netto di 60 litri ed un valore di 6 dKH che vogliamo portare a 4 dKH à
- 6 x 60 = 4 x C2 -> 60×40/6 -> C2=40
- 60 – 40 = 20 sono i litri di acqua dell’ acquario che dobbiamo sostituire con RO per abbassare il KH da 6dKH a 4dKH.
ATTENZIONE: Quando si opera un abbassamento del KH con cambi parziali tenete presente che inevitabilmente andremo a ridurre anche il GH per cui dobbiamo tenere conto anche di questa variabile e correggerla con gli appositi sali in commercio o soluzioni DYI (preferire il MgSO4 o una miscela di questo con il CaCl2).
Alzare il KH: in commercio ci sono molti prodotti per alzare solo il KH (Alkalyne Buffer Seachem, Sera KH/Ph Plus, etc.). Per gli amanti del DYI si suggerisce di usare l’idrogeno carbonato di potassio (KHCO3). Da evitare assolutamente il corrispettivo sale di sodio (Na). Quindi procuratevi i sali di KHCO3 ma mi raccomando che siano sali con purezza 99%.
3,57 gr di KHCO3 in 100 litri aumentano il KH di 1 dKH.
I sali possono essere sciolti in un litro di acqua della vasca e poi reintrodotti usando un piccolo tubicino in modo da far aumentare lentamente la durezza.
Una attenzione per chi usa fondi allofani. Questi fondi caratterizzati da una particolare reattività presentano una CSC (capacità di scambio cationico) molto alta per cui assorbono i cationi liberando idrogenioni dando così vita alla seguente reazione
H+ + HCO3– -> H2CO3 -> H2O + CO2 (gas)
Questo spiega perché questi fondi tendono ad abbassare il KH. I fondi allofani sono capaci di azzerare il KH per un periodo piuttosto lungo (attività molto gradita per gli allevatori di C. cantonensis) mantenendo allo stesso tempo un pH acido (6.0 – 6.5). Un trucco per beneficiare di tutti gli effetti di questi fondi senza incorrere in abbassamenti drastici di KH è quello d’ inserire nel layout rocce Seiryu che grazie alle loro venature di carbonati impediscono al KH di scendere troppo.
CaCO3 + H+ -> HCO3– + Ca2-
Il fondo allofano assorbe i cationi (Ca, Mg, etc.) liberando ioni idrogeno che interagiscono con l’ idrogenocarbonato (quindi il KH si abbassa) formando acido carbonico che come acido attacca il carbonato di calcio della Seiryu stone liberando idrogeno carbonato (quindi il KH si alza) e calcio che a sua volta viene riassorbito dall allofano creando un circolo che trova il suo equilibrio con un KH i cui valori possono diversificare a secondo della maggiore o minore reattività del fondo ma non andranno mai a 0.
La durezza GH
La durezza dell’acqua esprime il contenuto dei sali di Ca e Mg ma anche di eventuali metalli pesanti. Il contenuto di tutti questi sali esprime la durezza totale. In acquariologia si fa riferimento per la durezza totale al contenuto di Ca e Mg in quanto sono gli elementi principali e più abbondanti legati allo stato solido a diversi anioni (SO42-, HCO3–, CO32-, Cl–, etc.). Essa viene indicata con il simbolo GH.
Abbiamo poi la durezza temporanea che esprime il contenuto di idrogenocarbonati (HCO3–) prima dell’ebollizione. La temporaneità sta nel fatto che se facciamo bollire l’acqua gli idrogenocarbonati si trasformano in carbonati di calcio e magnesio che a causa della loro scarsa solubilità precipitano. In acquario quando l’acqua evapora si forma sui vetri quella striscia di colore biancastro: quello è carbonato di calcio e magnesio (CaCO3 e MgCO3). Questa durezza viene indicata con il simbolo KH. Abbiamo una terza durezza denominata permanente ed è costituita da tutti i cationi rimasti in acqua dopo una lunga ebollizione. Questa durezza non trova applicazione in acquariologia.
Il GH
La durezza dell’acqua sia essa di rete che minerale viene espressa in gradi francesi °f mentre in acquariologia si usano i gradi tedeschi dGH. Il fattore di conversione che ci permette di calcolare dai gradi francesi che rappresentano il contenuto in CaCO3 i gradi tedeschi che esprimono il contenuto di CaO è 1,785. Quindi abbiamo
dGH=°f/1,785.
Quindi un’acqua che ha una durezza di 10 °f corrisponde a 5,6 dGH. Questa formula vi aiuta a determinare la durezza in dGH della vostra acqua di rete. La durezza totale è rappresentata dalla quantità di Ca e Mg presenti in acqua essendo questi gli elementi preponderanti al punto tale da rendere trascurabile il peso degli altri elementi. Ancora una volta possiamo arrivare al valore del GH conoscendo il contenuto di Ca e Mg dell’acqua (ricordate che su internet potete trovare le analisi dell’acqua distribuita dal vostro comune anche se i valori possono essere fluttuanti nel tempo a seguito dei periodi stagionali che possono modificare le fonti di approvvigionamento.
dGH= peso del Ca + peso del Mg/6,32
Le variabili dGH, Ca e Mg e la costante fissa 6,32 ci permettono di calcolare una variabile conoscendo le altre due.
Tabella delle durezze espresse in dGH
- fino a 2,2°: molto dolci
- da 2,2° a 4,5°: dolci
- da 4,5° a 6,7°: medio-dure
- da 6,7 ° a 10°: discretamente dure
- da 10° a 16,8°: dure
- oltre 16,8°: molto dure.
Attenzione: quando trovate il valore del GH dell’acqua di rete inferiore a quello del KH questo significa che l acqua presenta concentrazioni alte di NaHCO3 (bicarbonati di sodio) e quindi l’eccesso di sodio potrebbe avere effetti negativi sulle piante sensibili a concentrazioni superiori ai 40 ppm (mg/lt).
Un po’ di biologia: il Gh è un parametro importante da valutare perché le concentrazioni di Ca e Mg possono influire positivamente o negativamente sullo stato di benessere e di crescita sia degli animali ma anche delle piante. Una mancanza di Ca può indurre nelle piante una deformazione delle foglie apicali che si presentano piccole e dall’ aspetto deformato mentre una carenza del magnesio che rientra nella struttura molecolare della clorofilla influisce negativamente sulla sintesi clorofilliana e si manifesta con una clorosi atipica che va dall’ esterno verso il centro e a differenza di quella indotta da carenza di ferro non interessa le nervature che restano verdi. Carenze di calcio possono essere responsabili della fragilità delle conchiglie delle lumache o di interferire sui processi biologici degli animali.
Correggere il GH Quando vi trovate a correggere il GH per alzarlo potete fare ricorso a diversi preparati in polvere o liquidi messi in commercio dalle ditte del settore. Per gli amanti del DIY potete usare il MgSO4, detto sale inglese, facilmente reperibile come sale puro nelle farmacie per meno di un euro oppure ricorrere ad una miscela di questo con il CaCl2.
Poiché il Mg è quello maggiormente consumato dalle piante correggere il GH con il corrispettivo sale non è una metodica errata.
Il sale inglese è solfato di magnesio epta idrato per cui occorreranno circa 6,5 gr per alzare il GH di 1dGH in 100 litri di acqua.
Per abbassare il GH si ricorre a cambi parziali fatti con sola acqua osmotica (RO = reverse osmosis) ma ricordatevi che l’abbassamento del GH operando una diluizione con RO inevitabilmente abbasserà anche il KH che dovrà poi essere corretto.
Per applicare i calcoli di diluizione per abbassare il GH potete fare ricorso alla stessa operazione descritta per il KH inserendo ovviamente i dati del GH al posto di quelli per il KH.
Alcune foto sono state prese dal web , qualora il proprietario le riconoscesse come proprietario e ne vuole la rimozione basta comunicarcelo e provvederemo immediatamente all’ eliminazione.
Testo: © Mario Mandici per Zio Pesce.blog – ogni riproduzione vietata senza il consenso dell’autore
Foto © Maurizio Vendramini per Zio Pesce.blog – ogni riproduzione vietata



Salve
vorrei sapere cosa comporta un eccesso di magnesio su molti tesi si legge che il rapporto con il calcio dovrebbe essere di 1a4, io da sempre ho tale rapporto quasi a parti invertite a favore del magnesio.
Dalla formula Gh-Gh/Ca = Gh/Mg. Esempio Gh 9 Ca 35 ppm (35/7.158 = 4.889 Gh/Calcio) quindi 9- 4.889 = 4.111 di Gh solo magnesio,
quindi 4.11 x 4.341 = 17.841 ppm di magnesio quindi ricapitolando calcio 35 ppm magnesio 18 ppm arrotondato per eccesso.
Rapporto Ca/Mg 1,9 quidi molto sbilaciato a favore del magnesio. Ho provato a tirare su il Gh con solo Ca con soluzioni a base di solfato di calcio (CaSO4) ma proporzionalmente mi si alza sempre anche Mg e il rapporto non cambia.
Le piante sembra che soffrino di una carenza di Ca.
Ciao ti riporto direttamente la risposta dell’autore Mario Mandici. Rimaniamo a disposizione per eventuali chiarimenti. Puoi anche contattarmi tramite mail.
Premesso che il rapporto Ca:Mg è di 4:1 i nuovi orientamenti nella fertilizzazione suggeriscono un rapporto di 3:1. Il Ca svolge un ruolo fondamentale nella divisione cellulare per cui una sua carenza influisce sullo sviluppo della lamina fogliare ma non sulle nervature per cui le foglie apicali crescono piccole ed accartocciate sui margini fogliari. Il Mg invece è il core della clorofilla, è l’ unico elemento inorganico che costituisce questa molecola fondamentale per la fotosintesi clorofilliana. A differenza del Mg il Ca entra più facilmente in acquario ed è meno consumato per cui è più facile avere una carenza da Mg che non da Ca. Per valori di GH = o > di 3 dGH è molto difficile osservare una carenza da Ca. Conoscendo il GH ed uno dei due elementi la formula più semplice è GH= Ca+Mg/6,32. Usando i tuoi numeri il rapporto Ca/Mg=1,6. Un eccesso di Mg non comporta nessun problema se non quello di alzare il GH diversamente un eccesso di Ca inibisce l’ assorbimento del Mg e quindi le piante rispondono con segnali che ricordano la carenza di Mg. Fermo restando che il CaSO4 ha una bassa solubilità pari a 2,6 gr/L a 25 °C non è possibile chimicamente parlando che l’ uso di questo sale possa aumentare il Mg ma solo il GH a mene che tu non utilizzi fertilizzanti da giardino dove spesso al Ca è associato il Mg.